达克罗表面涂层为何能防锈?专业的为你解密!
作者:
杭州赫格纳斯
【
原创
】
2020-07-02
达克罗表面涂层为何能防锈?专业的为你解密!
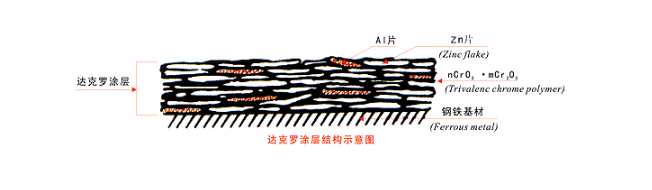
一、达克罗涂层的构造简图:
达克罗表面处理达克罗表面处理
二、防锈机理:
1.达克罗涂层为多层鳞片状锌、铝片层层叠加而成,减缓了腐蚀介质的渗入速度。
2.锌、铝片相对铁电极电位较负,可充当牺牲性阳极保护(电镀锌相同)。
3.锌、铝片处于受控的钝化状态,腐蚀速率慢。
4.涂层中有适量的可溶性六价铬,在遇到电解质溶液时,会形成铬酸,再次钝化锌、铝片等(自我修复作用)。

三、与电镀锌防锈机理区别:
1.涂层中的每层锌,铝片都处于钝化状态,而电镀锌只有最外层有0.05~0.2um的钝化层。
2.涂层中的锌、铝片起到充分的牺牲阳极保护作用,而电镀锌层会出现钝化层遭破坏后的锌浪费现象。
3.涂层及涂液中的铬盐在对锌铝保护时,同时钝化保护铁基体,而电镀锌没有。
4.镀锌层钝化层在70~100℃时,结晶水开始挥发,造成钝化层龟裂,影响镀锌层耐蚀性能,而达克罗涂层在300℃左右条件下烧结,所以无此类现象。
四、钝化保护:
为了提高锌层或锌片的防腐蚀性能与附着力,将其在含有六价铬或三价铬的铬酸盐溶液中处理,在其表面形成较密的氧化膜,也叫做钝化膜。
钝化膜结构:
1.通式:mCrO3·nCr2O3(达克罗)
xCrO3.yCr2O3.ZH2O(电镀锌)
2.专业实际:Cr2O3.(HOH)CrO4.Cr2CrO4.Zn2(OH)2CrO4.Zn(CrO2)2
3.钝化膜中三价铬强度高,稳定性好,形成网状结构,与基体形成化学键结合,提高附着力;六价铬主要通过夹杂、吸附、化学键结合存在于三价铬的网状结构中,当基体遭到电解质溶液破坏时,六价铬会形成铬酸,自我修复。
阅读
推荐
-

-

QQ空间
-

新浪微博
-

人人网
-

豆瓣




